In de groep van Medische Cel Biologie, produceren en werken we
met Humaan geïnduceerde pluripotente stamcellen (IPSCs)
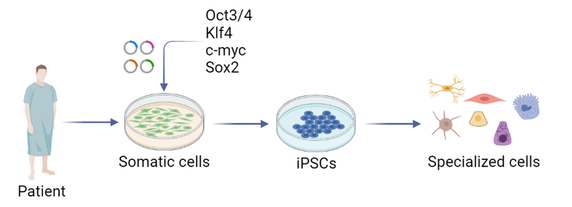
- Stamcellen zijn van enorme waarde voor regeneratieve geneeskunde. Deze cellen vernieuwen zich voor onbepaalde tijd en kunnen differentiëren in bijna elk celtype in het menselijk lichaam. Humane embryonale stamcellen worden al tientallen jaren gebruikt, maar meer recentelijk hebben IPSCs een revolutie teweeggebracht op het gebied van regeneratieve geneeskunde. Deze geïnduceerde stamcellen bieden veel voordelen: ze brengen minder ethische bezwaren met zich mee en vertonen de genetische achtergrond van de donorpatiënt. IPSCs worden direct gegenereerd in ons lab, met behulp van een integratievrije herprogrammeringsaanpak. Invasieve monsterafname van de patiënt wordt vermeden door te werken met een eenvoudig urinemonster. Geëxfolieerde nierepitheelcellen worden geïsoleerd en geëxpandeerd uit het urinemonster en dienen als uitstekend uitgangsmateriaal voor herprogrammering. De commerciële Sendai Cytotune 2.0 kit (Life Technologies) wordt gebruikt voor maximale efficiëntie en betrouwbaarheid.
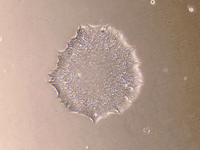
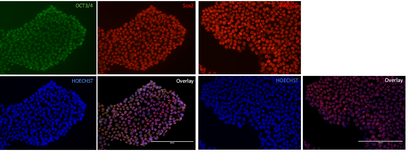
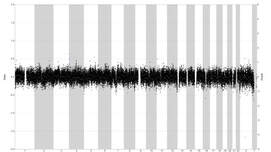
- De gegenereerde IPSCs ondergaan een uitgebreide kwaliteitscontrole. We controleren morfologie met behulp van microscopie, de kolonies zijn rond en dicht opeen gepakt, met gladde randen en een transparant lichaam. Pluripotentie wordt bevestigd door kleuring voor specifieke factoren, zoals POU5F1, NANOG en SOX2. Shallow whole genome sequencing (SWGS) zal ons waarschuwen in geval van genomische afwijkingen, zoals deleties of duplicaties. Het differentiatiepotentieel wordt bevestigd door de IPSCs te richten op de drie verschillende kiemlijnen, die met behulp van PCR worden gevalideerd. De pathogene variant van interesse (indien aanwezig) wordt gecontroleerd met behulp van Sanger-sequencing.
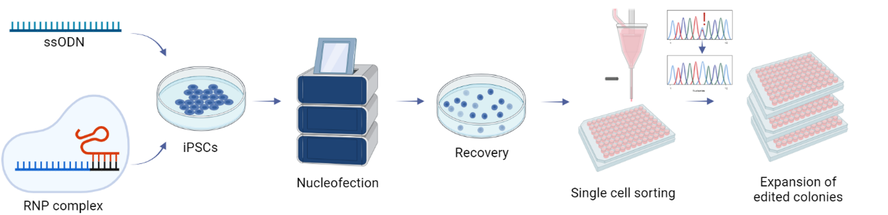
- Met de opkomst van CRISPR genome editing kunnen we precieze veranderingen in het genoom aanbrengen. Zo kunnen we ziekteverwekkende varianten in het genoom corrigeren. In ons lab gebruiken we de volgende workflow, waarbij we een gecomplexeerd Cas9 toevoegen, het eiwit dat het DNA knipt met het enkele gids-RNA, dat de doellocatie van belang herkent. Naast dit RNP-complex voegen we een enkelstrengs oligodeoxynucleotide-reparatiesjabloon toe door middel van nucleofectie. Wanneer Cas9 een dubbele strengbreuk introduceert, zal de cel proberen deze breuk te repareren door een proces dat NHEJ (niet-homologe eindverbinding) wordt genoemd. Dit proces is echter gevoelig voor fouten, waardoor andere mutaties kunnen worden geïntroduceerd. Door een reparatiesjabloon te leveren, gebruikt de cel een alternatieve, preciezere reparatiemethode: homologie gerichte reparatie. Na herstel worden de cellen één voor één gesorteerd in een nieuwe put, om monoklonaliteit te garanderen. Reparatie van de beoogde pathogene variant wordt geëvalueerd, waarna de succesvol gecorrigeerde klonen verder worden uitgebreid en onderworpen aan dezelfde karakterisering als hierboven beschreven. Deze gegenereerde lijnen dienen als isogene controles, met een identieke genetische achtergrond (afgezien van de gecorrigeerde pathogene variant) als de zieke iPSC-lijn.
In de groep Medische Celbiologie genereren en werken we met runderembryonale stamcellen
- Runderembryonale stamcellen (bESCs) worden steeds belangrijker in zowel de regeneratieve geneeskunde als hun potentie voor de productie van kweekvlees. Net als iPSC's bezitten bESC's het vermogen om zich voor onbepaalde tijd te vernieuwen en te differentiëren in vrijwel elk celtype. Dit onbeperkte proliferatiepotentieel maakt ze van onschatbare waarde voor verschillende toepassingen. Afgeleid van embryo's in een vroeg stadium, delen bESC's dezelfde veelzijdige kenmerken als menselijke iPSC's, en bieden ze een robuust platform voor het bestuderen van ontwikkelingsprocessen en weefselregeneratie bij runderen. In de context van kweekvlees bieden bESC's een veelbelovende mogelijkheid voor het produceren van gestructureerd vlees van hoge kwaliteit door te differentiëren in spiercellen en andere weefseltypen. Het gebruik ervan in onderzoek blijft ons inzicht van celdifferentiatie en weefselregeneratie vergroten, waardoor de weg wordt vrijgemaakt voor innovatieve therapieën, diergeneeskundige behandelingen en oplossingen voor duurzame voedselproductie.
- De gegenereerde ESC's ondergaan een uitgebreide kwaliteitscontrole. We controleren hun morfologie met behulp van microscopie, die moet lijken op ronde, dicht opeen groeiende kolonies stamcellen, met gladde randen en een transparant lichaam. Pluripotentie wordt bevestigd door kleuring voor specifieke factoren, zoals POU5F1, NANOG en SOX2. Shallow Whole Genome Sequencing (SWGS) zal ons waarschuwen in geval van genomische afwijkingen, zoals deleties of duplicaties. Het differentiatiepotentieel wordt bevestigd door de ESC's te differentiëren naar de drie verschillende kiemlijnen, die worden gevalideerd met behulp van immunologie en qPCR.
- In ons laboratorium richten we ons op het verbeteren van spierrijping, hypertrofie en visco-elastische eigenschappen van weefsel door middel van stimulatie-experimenten op spierafgeleide myoblasten. We maken gebruik van gepulseerde elektromagnetische veldstimulatie (PEMFS) en mechanische stimulatie (MS). Voor de productie van gekweekt vlees gebruiken we bESC's of rundermyoblasten om te differentiëren tot spiercellen. PEMFS omvat stimulaties met korte intervallen om de fusiecapaciteit van myoblasten te verbeteren. MS wordt toegepast op 3D spierconstructies om de metabolische activiteit en verhoogde stijfheid te bevorderen, en om de vorming van myofibers bij runderen te stimuleren. Om gehele runderspierconstructies te visualiseren en te verwerken, gebruiken we optische clearingtechnieken zoals Cubic clearing en 3DISCO clearing. Deze methoden verbeteren de transparantie van het weefsel en vergemakkelijken de diepe penetratie van antilichamen, waardoor ons vermogen om de spierconstructies te bestuderen en te verfijnen wordt vergroot.